题目内容
如图,是金属活动性顺序表中铜、铁和铝元素被人类大规模开发、利用的大致年限.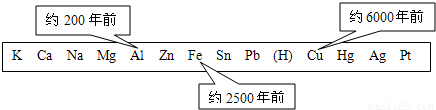
①铝的利用比铁、铜晚得多,这个事实与下列哪些因素有关.
A.铝在地壳中含量高;B.铝相对活泼;C.铝的硬度小;D.铝的冶炼相对难
②目前铝合金在多个领域替代易生锈的钢铁,其主要原因是.
③写出一个证明铁比铜活泼的化学方程式.
【答案】分析:①根据图示可发现,人类大规模开发、利用金属的先后顺序与金属活动必由强到弱的顺序正相反.据此猜测:金属越活泼越难以开发、利用;
②根据金属铝的性质,对比铝在防止锈蚀的优点;
③用化学方程式表示出铁比铜的活动性强,反应中应涉及这两种金属元素.
解答:解:①根据由题图所获得的信息,铝的利用晚于铁、铜是由于金属铝的活动性比铁、铜强,即选项B铝相对活泼;由于活动性较强,其冶炼则会相对比较困难.
故选B、D;
②铝的活动性较强,在常浊下可以与氧气反应生成氧化铝且形成致密的膜覆盖在铝的表面,隔绝金属铝与氧气的接触,防止了进一步氧化.
故答:铝的表面生成一层致密的氧化膜,对铝起到保护作用;
③铁的活动性比铜强,只要选择铁与可溶性的铜盐进行反应,即可证明铁比铜活泼.
故答:Fe+CuSO4=Cu+FeSO4
点评:防止金属锈蚀一般采取在金属表面涂一层保护膜的方法,用保护膜隔绝金属与氧气的接触.
②根据金属铝的性质,对比铝在防止锈蚀的优点;
③用化学方程式表示出铁比铜的活动性强,反应中应涉及这两种金属元素.
解答:解:①根据由题图所获得的信息,铝的利用晚于铁、铜是由于金属铝的活动性比铁、铜强,即选项B铝相对活泼;由于活动性较强,其冶炼则会相对比较困难.
故选B、D;
②铝的活动性较强,在常浊下可以与氧气反应生成氧化铝且形成致密的膜覆盖在铝的表面,隔绝金属铝与氧气的接触,防止了进一步氧化.
故答:铝的表面生成一层致密的氧化膜,对铝起到保护作用;
③铁的活动性比铜强,只要选择铁与可溶性的铜盐进行反应,即可证明铁比铜活泼.
故答:Fe+CuSO4=Cu+FeSO4
点评:防止金属锈蚀一般采取在金属表面涂一层保护膜的方法,用保护膜隔绝金属与氧气的接触.

练习册系列答案
相关题目




