题目内容
根据硝酸钾的溶解度曲线图回答下列问题.
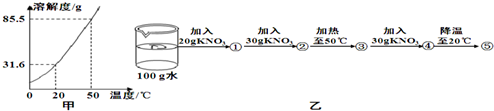
(1)从图甲可以得到的信息是
(2)欲将一瓶接近饱和的硝酸钾溶液变成饱和溶液,可采取的方法是
(3)某同学在20℃时进行了如图乙所示的实验,下列判断正确的是
A.④中溶质的质量分数最大 B.②⑤中溶质的质量分数相等
C.①③④中没有固体存在 D.②④⑤的溶液为饱和溶液.

(1)从图甲可以得到的信息是
硝酸钾溶解度随温度的升高而增大(其他合理答案均可)
硝酸钾溶解度随温度的升高而增大(其他合理答案均可)
(写出一条即可).(2)欲将一瓶接近饱和的硝酸钾溶液变成饱和溶液,可采取的方法是
降低温度(或蒸发溶剂或增加溶质)
降低温度(或蒸发溶剂或增加溶质)
(写出一种即可).(3)某同学在20℃时进行了如图乙所示的实验,下列判断正确的是
ABC
ABC
.A.④中溶质的质量分数最大 B.②⑤中溶质的质量分数相等
C.①③④中没有固体存在 D.②④⑤的溶液为饱和溶液.
分析:(1)由溶解度曲线可知物质的溶解度随温度变化情况,某温度下物质的溶解度等;
(2)不饱和溶液变为饱和溶液的一般方法是:增加溶质、蒸发溶剂、降温;
(3)据硝酸钾在20℃、50℃时的溶解度及溶质的质量分数计算方法、饱和溶液的判断分析解答.
(2)不饱和溶液变为饱和溶液的一般方法是:增加溶质、蒸发溶剂、降温;
(3)据硝酸钾在20℃、50℃时的溶解度及溶质的质量分数计算方法、饱和溶液的判断分析解答.
解答:解:(1)从图甲可以知道:硝酸钾的溶解度随温度的升高而增大,20℃时硝酸钾的溶解度是31.6g等;
(2)硝酸钾的溶解度随温度的升高而增大,欲将一瓶接近饱和的硝酸钾溶液变成饱和溶液,可采取增加硝酸钾、蒸发水、降温的方法;
(3)分析乙图:①是向100g水中加入20g硝酸钾,是不饱和溶液,②是100g水中加入了50g硝酸钾,最多溶解31.6g,是饱和溶液,③是升温至50℃,此时硝酸钾的溶解度是85.5g,此时形成的是不饱和溶液,溶质的质量是50g;④再加入30g硝酸钾,溶质质量是80g,形成的是不饱和溶液;降温至20℃,形成的是饱和溶液,饱和溶液中溶质的质量分数是:
×100%;
A、根据以上分析可知:④中溶质的质量最多,溶质的质量分数最大,正确;
B、②⑤都是20℃时硝酸钾的饱和溶液,故溶质的质量分数相等,正确;
C、①③④是硝酸钾在此温度下的不饱和溶液,故没有固体存在,正确;
D、通过以上分析可知:④形成的是不饱和溶液,故错误;
故答案为:
(1)硝酸钾溶解度随温度的升高而增大(其他合理答案均可);
(2)降低温度(或蒸发溶剂或增加溶质);
(3)ABC.
(2)硝酸钾的溶解度随温度的升高而增大,欲将一瓶接近饱和的硝酸钾溶液变成饱和溶液,可采取增加硝酸钾、蒸发水、降温的方法;
(3)分析乙图:①是向100g水中加入20g硝酸钾,是不饱和溶液,②是100g水中加入了50g硝酸钾,最多溶解31.6g,是饱和溶液,③是升温至50℃,此时硝酸钾的溶解度是85.5g,此时形成的是不饱和溶液,溶质的质量是50g;④再加入30g硝酸钾,溶质质量是80g,形成的是不饱和溶液;降温至20℃,形成的是饱和溶液,饱和溶液中溶质的质量分数是:
| 溶解度 |
| 溶解度+100g |
A、根据以上分析可知:④中溶质的质量最多,溶质的质量分数最大,正确;
B、②⑤都是20℃时硝酸钾的饱和溶液,故溶质的质量分数相等,正确;
C、①③④是硝酸钾在此温度下的不饱和溶液,故没有固体存在,正确;
D、通过以上分析可知:④形成的是不饱和溶液,故错误;
故答案为:
(1)硝酸钾溶解度随温度的升高而增大(其他合理答案均可);
(2)降低温度(或蒸发溶剂或增加溶质);
(3)ABC.
点评:了解饱和溶液的概念、物质的溶解度曲线的意义等知识并会灵活运用分析解答相关问题.

练习册系列答案
相关题目
 ,用化学符号表示为
,用化学符号表示为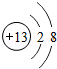 ,用化学符号表示为
.
,用化学符号表示为
.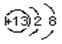 , 用化学符号表示为_________。
, 用化学符号表示为_________。