题目内容
一次课外小组活动,老师拿出一瓶溶质质量分数为10%的无色溶液,和同学们一起探究其溶质的成分.
【提出猜想】老师提示该溶液只能是下列四种溶液中的一种:
①NH4Cl ②Na2CO3 ③稀盐酸 ④Ca(OH)2
【查阅资料】NH4Cl、Na2CO3 易溶于水,NH4Cl溶液显酸性,常温下Ca(OH)2的溶解度小于1g.
【交流讨论I】同学们一致认为该溶液不是________(填序号)
【活动探究】同学们设计了一下三个实验方案
| 实验方案 | 现象 | 结论 |
| 方案一:取少量溶液向其中滴加CaCl2溶液 | 若________ | 猜想2成立反应的化学方程式是________ |
| 方案二:取少量溶液向其中滴加石蕊溶液 | 若溶液变红 | 猜想3成立 |
| 方案三:取少量溶液向其中滴加氢氧化钠溶液 | 若有刺激性气味的气体生成 | 猜想________成立,反应的化学方程式是________ |
小丽认为只有一种试剂一次性就能完成上述【活动探究】从而确定溶液名称,他用的试剂是________.
④ 有白色沉淀 CaCl2+Na2CO3=CaCO3↓+2NaCl ① NaOH+NH4Cl=NaCl+H2O+NH3↑ 氯化铵溶液也显酸性 氢氧化钙溶液或氢氧化钡溶液
分析:通过分析可知:该溶液不是氢氧化钙,因为常温下Ca(OH)2的溶解度小于1g,因此氢氧化钙溶液中溶质质量分数<10%;方案一:取少量溶液向其中滴加CaCl2溶液,若有白色沉淀生成,一定有碳酸钠,因为碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,配平即可.酸能使紫色石蕊试液变红色;方案三:取少量溶液向其中滴加氢氧化钠溶液,若有刺激性气味的气体生成,说明有氯化铵;氯化铵的氢氧化钠溶液反应生成氯化钠和水和氨气;小红认为方案二结论不合理,理由是氯化铵溶液也显酸性;方案一用的是钙离子,方案三用的是氢氧根离子,因此我们可以用氢氧化钙溶液,从而确定溶液名称.
解答:(1)【交流讨论I】通过分析可知:该溶液不是氢氧化钙,因为常温下Ca(OH)2的溶解度小于1g,因此氢氧化钙溶液中溶质质量分数<10%,故答案为:④
(2)【活动探究】方案一:取少量溶液向其中滴加CaCl2溶液,若有白色沉淀生成,一定有碳酸钠,因为碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,配平即可.酸能使紫色石蕊试液变红色;方案三:取少量溶液向其中滴加氢氧化钠溶液,若有刺激性气味的气体生成,说明有氯化铵;氯化铵的氢氧化钠溶液反应生成氯化钠和水和氨气,故答案为:有白色沉淀; CaCl2+Na2CO3=CaCO3↓+2NaCl;①;NaOH+NH4Cl=NaCl+H2O+NH3↑
(3)【交流讨论II】小红认为方案二结论不合理,理由是氯化铵溶液也显酸性;方案一用的是钙离子,方案三用的是氢氧根离子,因此我们可以用氢氧化钙溶液,从而确定溶液名称,氢氧化钡溶液也有相同的现象,故答案为:氯化铵溶液也显酸性;氢氧化钙溶液或氢氧化钡溶液;
点评:实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.
分析:通过分析可知:该溶液不是氢氧化钙,因为常温下Ca(OH)2的溶解度小于1g,因此氢氧化钙溶液中溶质质量分数<10%;方案一:取少量溶液向其中滴加CaCl2溶液,若有白色沉淀生成,一定有碳酸钠,因为碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,配平即可.酸能使紫色石蕊试液变红色;方案三:取少量溶液向其中滴加氢氧化钠溶液,若有刺激性气味的气体生成,说明有氯化铵;氯化铵的氢氧化钠溶液反应生成氯化钠和水和氨气;小红认为方案二结论不合理,理由是氯化铵溶液也显酸性;方案一用的是钙离子,方案三用的是氢氧根离子,因此我们可以用氢氧化钙溶液,从而确定溶液名称.
解答:(1)【交流讨论I】通过分析可知:该溶液不是氢氧化钙,因为常温下Ca(OH)2的溶解度小于1g,因此氢氧化钙溶液中溶质质量分数<10%,故答案为:④
(2)【活动探究】方案一:取少量溶液向其中滴加CaCl2溶液,若有白色沉淀生成,一定有碳酸钠,因为碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,配平即可.酸能使紫色石蕊试液变红色;方案三:取少量溶液向其中滴加氢氧化钠溶液,若有刺激性气味的气体生成,说明有氯化铵;氯化铵的氢氧化钠溶液反应生成氯化钠和水和氨气,故答案为:有白色沉淀; CaCl2+Na2CO3=CaCO3↓+2NaCl;①;NaOH+NH4Cl=NaCl+H2O+NH3↑
(3)【交流讨论II】小红认为方案二结论不合理,理由是氯化铵溶液也显酸性;方案一用的是钙离子,方案三用的是氢氧根离子,因此我们可以用氢氧化钙溶液,从而确定溶液名称,氢氧化钡溶液也有相同的现象,故答案为:氯化铵溶液也显酸性;氢氧化钙溶液或氢氧化钡溶液;
点评:实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
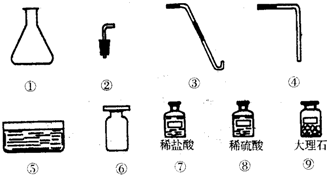 (2003?哈尔滨)在一次课外小组活动中,同学们想制取某种气体,化学老师为同学们提供了下列仪器及药品(如图)
(2003?哈尔滨)在一次课外小组活动中,同学们想制取某种气体,化学老师为同学们提供了下列仪器及药品(如图)