题目内容
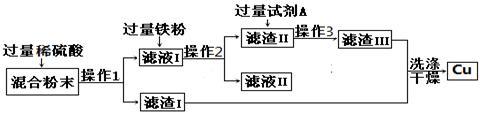
(7分)从铜、氧化铜的混合粉末中回收铜的具体流程如下:
回答下列问题:
(1)操作1是 。
(2)滤液Ⅰ中加入过量铁粉所发生的反应的化学方程式是
。
(3)试剂A的作用是 。
(4)此实验过程中,下列哪些做法会导致回收到的Cu不纯
A.往混合粉末中加入的稀H2SO4不足
B.往滤液Ⅰ中加入铁粉不足
C.往滤渣Ⅱ中加入试剂A不足
(5)请写出铜的一种用途: 。

回答下列问题:
(1)操作1是 。
(2)滤液Ⅰ中加入过量铁粉所发生的反应的化学方程式是
。
(3)试剂A的作用是 。
(4)此实验过程中,下列哪些做法会导致回收到的Cu不纯
A.往混合粉末中加入的稀H2SO4不足
B.往滤液Ⅰ中加入铁粉不足
C.往滤渣Ⅱ中加入试剂A不足
(5)请写出铜的一种用途: 。
(1)过滤 (2)Fe + H2SO4 ="==" FeSO4 + H2↑ Fe+CuSO4==Cu+FeSO4
(3)除去滤渣Ⅱ中过量的铁粉 (4)C (5)做导线
(3)除去滤渣Ⅱ中过量的铁粉 (4)C (5)做导线
试题分析:(1)操作1是将滤液和滤渣进行分离,所以是过滤
(2)在混合粉末中加入过量的硫酸,所以在滤液Ⅰ中既有生成的硫酸铜,还有过量的硫酸,所以滤液Ⅰ中加入过量铁粉所发生的反应的化学方程式是:Fe + H2SO4 ="==" FeSO4 + H2↑ Fe+CuSO4==Cu+FeSO4
(3)由于所加的铁粉是过量的,所以滤渣Ⅱ中是铁和铜的混合物,所以试剂A的作用是:除去滤渣Ⅱ中过量的铁粉
(4)此实验过程中,会导致回收到的Cu不纯往滤渣Ⅱ中加入试剂A不足,使得铁粉没有完全被反应
(5)铜的一种用途:做导线

练习册系列答案
相关题目