题目内容
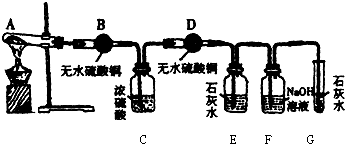 化学小组的同学对某粉末状物质进行分析.取8.0g该物质放入图中进行系列实验,结果如下:A中物质最后全部变为黑色;B中物质变为蓝色,B、C共增重0.9g;E中溶液变浑浊,E、F共增重1.1g;D、G中的物质无变化.反应结束后,将A中的黑色固体用氢气还原,黑色固体全部变红且有无色液体产生.
化学小组的同学对某粉末状物质进行分析.取8.0g该物质放入图中进行系列实验,结果如下:A中物质最后全部变为黑色;B中物质变为蓝色,B、C共增重0.9g;E中溶液变浑浊,E、F共增重1.1g;D、G中的物质无变化.反应结束后,将A中的黑色固体用氢气还原,黑色固体全部变红且有无色液体产生.请你根据实验结果,填写下列空白:
(1)B中无水硫酸铜变为蓝色,说明有
水
水
生成;D中无水硫酸铜的颜色不变,说明水已被完全吸收
水已被完全吸收
.(2)F中所发生反应的化学方程式为
2NaOH+CO2=Na2CO3+H2O
2NaOH+CO2=Na2CO3+H2O
.(3)原粉末状物质的组成元素是(填元素符号)
Cu、O、C、H
Cu、O、C、H
.(4)原粉末状物质中各元素的最简质量比为
Cu:O:C:H=48:28:3:1
Cu:O:C:H=48:28:3:1
.分析:根据题目给出的信息可知:B中无水硫酸铜是检验是否有水生成的;C中的浓硫酸是吸水干燥作用的;D中无水硫酸铜是检验水是否被完全吸收的;E是检验是否有二氧化碳生成的;F是吸收二氧化碳的;G是检验二氧化碳是否被完全吸收的;有关的计算要正确.
解答:解:(1)B中无水硫酸铜是检验是否有水生成的,D中无水硫酸铜是检验水是否被完全吸收的;故答案为:水;水已被完全吸收
(2)二氧化碳和氢氧化钠反应生成碳酸钠和水,配平即可,故答案为:2NaOH+CO2=Na2CO3+H2O
(3)A中物质最后全部变为黑色;B中物质变为蓝色;E中溶液变浑浊;将A中的黑色固体用氢气还原,黑色固体全部变红且有无色气体产生;因此生成物是:氧化铜和水和二氧化碳.故答案为:Cu、O、C、H
(4)B、C共增重0.9g,因此水是0.9g;E、F共增重1.1g,因此二氧化碳1.1g;因此氧化铜的质量=8.0g-0.9g-1.1g=6.0g;H的质量=0.9g×
=0.1g;C的质量=1.1g×
=0.3g;铜的质量=6.0g×
=4.8g;氧元素的质量=8.0g-4.8g-0.1g-0.3g=2.8g;故答案为:Cu:O:C:H=48:28:3:1
(2)二氧化碳和氢氧化钠反应生成碳酸钠和水,配平即可,故答案为:2NaOH+CO2=Na2CO3+H2O
(3)A中物质最后全部变为黑色;B中物质变为蓝色;E中溶液变浑浊;将A中的黑色固体用氢气还原,黑色固体全部变红且有无色气体产生;因此生成物是:氧化铜和水和二氧化碳.故答案为:Cu、O、C、H
(4)B、C共增重0.9g,因此水是0.9g;E、F共增重1.1g,因此二氧化碳1.1g;因此氧化铜的质量=8.0g-0.9g-1.1g=6.0g;H的质量=0.9g×
| 2 |
| 18 |
| 12 |
| 44 |
| 64 |
| 80 |
点评:本考点属于实验探究题,既可以根据实验现象推断物质,又可以根据质量进行有关的计算,还有化学方程式的书写,综合性比较强.本题根据题目提供的信息,结合实验探究的一般步骤和物质的检验方法等知识来解决,还要注意化学方程式的书写和配平.本考点主要出现在实验题中.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目