题目内容
碘是人体必须得一种微量元素.碘元素的符号为I,图1是I-(碘离子)的结构示意图.
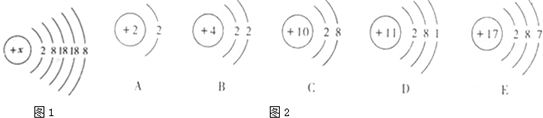
(1)图1中x=________.
(2)碘属于________元素(填“金属”或“非金属”).图2表示的微粒中,与I化学性质相似的是________(填字母序号)
解:(1)由于I-是碘原子得到一个电子形成的,在原子中,核河内的质子数等于核外的电子数.所以,X=2+8+18+18+8-1=53;
(2)碘元素的汉字名称中在带“石”字旁,属于非金属元素,最外层电子数是7,由于决定元素化学性质的是最外层电子数,E的最外层是7,所以与I化学性质相似的是E.
故答为:(1)53;(2)非金属,E.
分析:(1)根据原子和离子之间的关系及质子数与核外电子数的关系判断X的值;
(2)根据元素名称的判断元素的类别,根据原子结构的特点与元素化学性质的关系判断具有相似性质的微粒.
点评:解答本题关键是要知道原子结构示意图中核内质子数等于核外电子数,知道金属元素、非金属元素的判断方法,知道相对稳定结构的特点.
(2)碘元素的汉字名称中在带“石”字旁,属于非金属元素,最外层电子数是7,由于决定元素化学性质的是最外层电子数,E的最外层是7,所以与I化学性质相似的是E.
故答为:(1)53;(2)非金属,E.
分析:(1)根据原子和离子之间的关系及质子数与核外电子数的关系判断X的值;
(2)根据元素名称的判断元素的类别,根据原子结构的特点与元素化学性质的关系判断具有相似性质的微粒.
点评:解答本题关键是要知道原子结构示意图中核内质子数等于核外电子数,知道金属元素、非金属元素的判断方法,知道相对稳定结构的特点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某班同学在实验结束进行废弃物处理时,将生石灰、碳酸钠溶液倒入指定的洁净容器静置后,发现容器底部有白色不溶物存在,上层为无色清液.为了研究以上物质间的反应情况,他们决定对上层清液中溶质的组成进行探究.请写出可能发生的化学反应方程式(1)________;
(2)________.
[提出猜想](1)溶质为NaOH和Ca(OH)2;
(2)溶质为________;
(3)溶质为NaOH.
[验证猜想]可供选择的试剂①K2CO3溶液 ②Ba(NO3)2溶液 ③酚酞试液 ④FeCl3溶液
请你认真分析后填写完成实验报告,以证明猜想是正确的.
| 实验步骤 | 实验现象 | 实验结论 |
| 取上层清液于试管中,滴加________ | ________ | 猜想(1)成立 |
| 取上层清液于试管中,滴加________ | 有白色沉淀产生 | 猜想(2)成立 |
| ________ | ________ | 猜想(3)成立 |
