题目内容
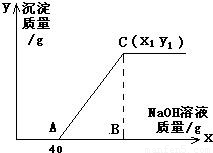
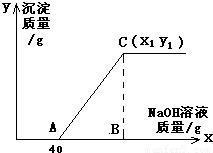
有盐酸和氯化铜的混合溶液共100g,向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液,生成的沉淀与加入的10%的氢氧化钠溶液的质量关系如如图所示.若氯化铜在原混合溶液中的质量分数为13.5%.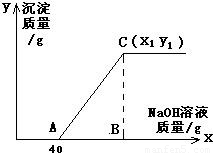
求:(1)原混合溶液中HCl的质量分数;
(2)C点的坐标(x1、y1)为多少?
【答案】分析:(1)所加入的氢氧化钠溶液一部分与稀盐酸发生中和反应,另一部分与氯化铜形成氢氧化铜沉淀;根据盐酸与氢氧化钠反应的化学方程式,由反应消耗氢氧化钠的质量计算所消耗盐酸中溶质的质量,利用溶质质量分数计算式求出混合溶液中HCl的质量分数;
(2)C点的坐标(x1、y1)中x1为总共消耗氢氧化钠溶液的质量、y1为生成沉淀氢氧化铜的质量;根据氢氧化钠与氯化铜反应的化学方程式,可由氯化铜的质量计算出与之发生反应的氢氧化钠的质量及生成的沉淀氢氧化铜的质量y1;由氢氧化钠的质量与氢氧化钠溶液的质量分数计算出与氯化铜反应的氢氧化钠溶液的质量,该质量加上与稀盐酸反应氢氧化钠溶液质量40g即为整个过程所消耗氢氧化钠溶液的总质量x1.
解答:解:(1)由关系图可知,与混合溶液中盐酸发生反应的氢氧化钠溶液的质量为40g,其中氢氧化钠的质量=40g×10%=4g;
设反应消耗HCl的质量为x
NaOH+HCl═NaCl+H2O
40 36.5
4g x
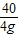 =
=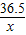 x=3.65g
x=3.65g
原混合溶液中HCl的质量分数=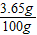 ×100%=3.65%
×100%=3.65%
(2)混合溶液中含氯化铜的质量=100g×13.5%=13.5g
设反应消耗氢氧化钠的质量为y,反应生成沉淀氢氧化铜的质量为y1
CuCl2+2NaOH═Cu(OH)2↓+2NaCl
135 80 98
13.5g y y1
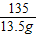 =
=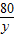 y=8g
y=8g
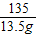 =
=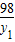 y1=9.8g
y1=9.8g
整个过程所消耗氢氧化钠溶液的总质量x1=40g+8g÷10%=120g
答:(1)原混合溶液中HCl的质量分数为3.65%;(2)C点的坐标为(120,9.8).
点评:在对表示反应过程的曲线进行分析时,该曲线的起点表示氢氧化钠恰好与盐酸完全反应,曲线的折点为与氯化铜恰好完全反应.
(2)C点的坐标(x1、y1)中x1为总共消耗氢氧化钠溶液的质量、y1为生成沉淀氢氧化铜的质量;根据氢氧化钠与氯化铜反应的化学方程式,可由氯化铜的质量计算出与之发生反应的氢氧化钠的质量及生成的沉淀氢氧化铜的质量y1;由氢氧化钠的质量与氢氧化钠溶液的质量分数计算出与氯化铜反应的氢氧化钠溶液的质量,该质量加上与稀盐酸反应氢氧化钠溶液质量40g即为整个过程所消耗氢氧化钠溶液的总质量x1.
解答:解:(1)由关系图可知,与混合溶液中盐酸发生反应的氢氧化钠溶液的质量为40g,其中氢氧化钠的质量=40g×10%=4g;
设反应消耗HCl的质量为x
NaOH+HCl═NaCl+H2O
40 36.5
4g x
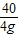 =
=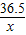 x=3.65g
x=3.65g原混合溶液中HCl的质量分数=
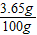 ×100%=3.65%
×100%=3.65%(2)混合溶液中含氯化铜的质量=100g×13.5%=13.5g
设反应消耗氢氧化钠的质量为y,反应生成沉淀氢氧化铜的质量为y1
CuCl2+2NaOH═Cu(OH)2↓+2NaCl
135 80 98
13.5g y y1
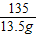 =
=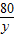 y=8g
y=8g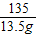 =
=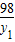 y1=9.8g
y1=9.8g整个过程所消耗氢氧化钠溶液的总质量x1=40g+8g÷10%=120g
答:(1)原混合溶液中HCl的质量分数为3.65%;(2)C点的坐标为(120,9.8).
点评:在对表示反应过程的曲线进行分析时,该曲线的起点表示氢氧化钠恰好与盐酸完全反应,曲线的折点为与氯化铜恰好完全反应.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
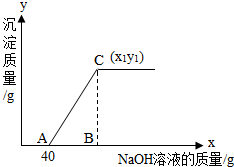 有盐酸和氯化铜的混合溶液共100g,向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液,生成的沉淀与加入的10%的氢氧化钠溶液的质量关系如如图所示.若氯化铜在原混合溶液中的质量分数为13.5%.
有盐酸和氯化铜的混合溶液共100g,向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液,生成的沉淀与加入的10%的氢氧化钠溶液的质量关系如如图所示.若氯化铜在原混合溶液中的质量分数为13.5%.