题目内容
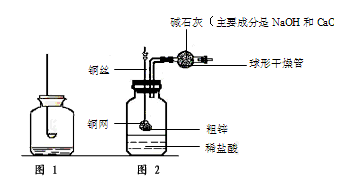
小钱和小鸣同学在实验室里进行的一些化学探究实验,下图是他们进行实验的一些装置图.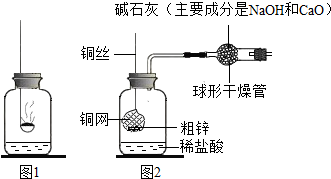
(1)他们利用图1装置探究质量守恒定律的实验,实验过程如下表.
| 实验过程 | 实验数据记录 |
| 在瓶底放入少量盐酸,将少量大理石粉末放在燃烧匙上,塞紧橡皮塞. | 应记录的实验数据是 |
| 将燃烧匙上的大理石粉末抖下,使其与盐酸接触. | 应记录的实验数据是 |
②小钱同学认为实验过程中缺少一个重要步骤,这个步骤是
③实验时
(2)他们还制作了一套如图2的装置,并用该装置测定粗锌样品的含锌量.
①称量10.0g粗锌放在铜网中,按图将仪器组装好以后,称得仪器和药品总质量为120.0g.②将铜网插人足量稀盐酸中,充分反应,可以观察到的实验现象为
③反应完全后,称得装置总质量为119.8g.则粗锌的纯度为
④该实验中碱石灰的作用是
⑤若将粗锌换成石灰石,原实验方案
分析:(1)创造密闭的反应装置,对反应前后物质的质量进行测量即可.
①因为反应中会生成大量的气体,所以会导致容器内的压强变大②因为该反应会生成气体,所以装置的气密性应很好.③该过程是用的是碳酸钙的粉末当然能与硫酸很好的反应.
(2)①②铜网不与盐酸反应,锌能与盐酸反应.③反应前后装置的质量差是氢气的质量,再利用方程式求解即可.
④碱石灰能吸收水蒸气与氯化氢气体,这样可使氢气的质量更准确一些.
⑤二氧化碳能与碱石灰反应,使产生气体的质量无法测量,所以该实验不可行.
①因为反应中会生成大量的气体,所以会导致容器内的压强变大②因为该反应会生成气体,所以装置的气密性应很好.③该过程是用的是碳酸钙的粉末当然能与硫酸很好的反应.
(2)①②铜网不与盐酸反应,锌能与盐酸反应.③反应前后装置的质量差是氢气的质量,再利用方程式求解即可.
④碱石灰能吸收水蒸气与氯化氢气体,这样可使氢气的质量更准确一些.
⑤二氧化碳能与碱石灰反应,使产生气体的质量无法测量,所以该实验不可行.
解答:解:(1)创造密闭的反应装置,对反应前后物质的质量进行测量,从而验证反应前后物质的质量变化.
①因为反应中会生成大量的气体,所以会导致容器内的压强变大,当达到一定程度时会把橡皮塞弹出.
②因为该反应会生成气体,所以装置的气密性应一定要很好,否则无法检验生成物的质量.
③由于该碳酸钙的粉末能与硫酸很好的反应,也可对质量守恒定律进行实验.
(2)①②铜网不与盐酸反应,锌能与盐酸反应生成氢气,因此实验时会有大量的气泡放出.
③反应前后装置的质量差是氢气的质量,生成氢气的质量是:120g-119.8g=0.2g
设反应的锌的质量是x
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.2g
=
x=6.5g
锌的质量分数=
×100%=65%
④碱石灰能吸收水蒸气与氯化氢气体,这样不会使其散出从而不会影响氢气的质量.
⑤二氧化碳能与碱石灰反应,使产生气体的质量无法测量,所以该实验不可行.
故答案为:(1)反应前所有物质和装置的总质量;反应后所有物质和装置的总质量
①产生气体的量太多,压强太大②检查装置气密性
③可以硫酸也能与石灰石发生化学反应,也能探究质量守恒定律
(2)②粗锌逐渐减少,有大量气泡产生Zn+2HCl=ZnCl2+H2↑③65%
④防止装置内的水分(稀盐酸挥发出的氯化氢气体)逃逸到空气中偏大
⑤不能碱石灰能吸收二氧化碳气体,从而无法测出生成的二氧化碳质量
①因为反应中会生成大量的气体,所以会导致容器内的压强变大,当达到一定程度时会把橡皮塞弹出.
②因为该反应会生成气体,所以装置的气密性应一定要很好,否则无法检验生成物的质量.
③由于该碳酸钙的粉末能与硫酸很好的反应,也可对质量守恒定律进行实验.
(2)①②铜网不与盐酸反应,锌能与盐酸反应生成氢气,因此实验时会有大量的气泡放出.
③反应前后装置的质量差是氢气的质量,生成氢气的质量是:120g-119.8g=0.2g
设反应的锌的质量是x
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.2g
| 65 |
| 2 |
| x |
| 0.2 |
x=6.5g
锌的质量分数=
| 6.5g |
| 10g |
④碱石灰能吸收水蒸气与氯化氢气体,这样不会使其散出从而不会影响氢气的质量.
⑤二氧化碳能与碱石灰反应,使产生气体的质量无法测量,所以该实验不可行.
故答案为:(1)反应前所有物质和装置的总质量;反应后所有物质和装置的总质量
①产生气体的量太多,压强太大②检查装置气密性
③可以硫酸也能与石灰石发生化学反应,也能探究质量守恒定律
(2)②粗锌逐渐减少,有大量气泡产生Zn+2HCl=ZnCl2+H2↑③65%
④防止装置内的水分(稀盐酸挥发出的氯化氢气体)逃逸到空气中偏大
⑤不能碱石灰能吸收二氧化碳气体,从而无法测出生成的二氧化碳质量
点评:该题是一道综合性较强的题目,解题时抓住质量守恒这一主线进行了分析与探讨,是一道训练学生思维与分析问题能力的中档题.

练习册系列答案
相关题目
小钱和小鸣同学在实验室里进行的一些化学探究实验,下图是他们进行实验的一些装置图.

(1)他们利用图1装置探究质量守恒定律的实验,实验过程如下表.
| 实验过程 | 实验数据记录 |
| 在瓶底放入少量盐酸,将少量大理石粉末放在燃烧匙上,塞紧橡皮塞. | 应记录的实验数据是______. |
| 将燃烧匙上的大理石粉末抖下,使其与盐酸接触. | 应记录的实验数据是______. |
②小钱同学认为实验过程中缺少一个重要步骤,这个步骤是______.
③实验时______(选填“可以”或“不可以”)用硫酸代替盐酸,原因是______.
(2)他们还制作了一套如图2的装置,并用该装置测定粗锌样品的含锌量.
①称量10.0g粗锌放在铜网中,按图将仪器组装好以后,称得仪器和药品总质量为120.0g.②将铜网插人足量稀盐酸中,充分反应,可以观察到的实验现象为______,反应的化学方程式______.
③反应完全后,称得装置总质量为119.8g.则粗锌的纯度为______.
④该实验中碱石灰的作用是______.若不用碱石灰,则所测定的粗锌纯度______(填“偏大”、“偏小”或“无影响”.不考虑空气中C02和H2O对实验的影响).
⑤若将粗锌换成石灰石,原实验方案______(填“能”或“不能”)用于石灰石样品纯度的测定,理由是______.
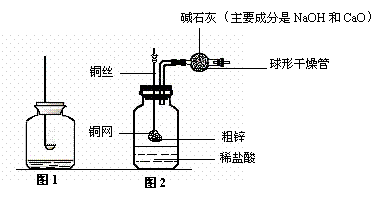 小钱和小鸣同学在实验室里进行的一些化学探究实验,下图是他们进行实验的一些装置图。
小钱和小鸣同学在实验室里进行的一些化学探究实验,下图是他们进行实验的一些装置图。
(1)他们利用图1装置探究质量守恒定律的实验,实验过程如下表。
| 实验过程 | 实验数据记录 |
| 在瓶底放入少量盐酸,将少量大理石粉末放在燃烧匙上,塞紧橡皮塞。 | 应记录的实验数据是________________。 |
| 将燃烧匙上的大理石粉末抖下,使其与盐酸接触。 | 应记录的实验数据是________________。 |
①实验中盐酸与大理石反应后出现橡皮塞被弹出来的情况,其可能的原因是___________。
②小钱同学认为实验过程中缺少一个重要步骤,这个步骤是_____________________ 。
③实验时______(选填“可以”或“不可以”)用硫酸代替盐酸,原因是___________ 。
(2)他们还制作了一套如图2的装置,并用该装置测定粗锌样品的含锌量。
①称量10.0g粗锌放在铜网中,按图将仪器组装好以后,称得仪器和药品总质量为120.0g。②将铜网插人足量稀盐酸中,充分反应,可以观察到的实验现象为____________________,反应的化学方程式______________________________。
③反应完全后,称得装置总质量为119.8g。则粗锌的纯度为___________。
④该实验中碱石灰的作用是___________________ _ 。若不用碱石灰,则所测定的粗锌纯度______(填“偏大”、“偏小”或“无影响” 。不考虑空气中![]() C02和H2O对实验的影响)。
C02和H2O对实验的影响)。
⑤若将粗锌换成石灰石,原实验方案_________(填“能”或“不能”)用于石灰石样品纯度的测定,理由是__________________________。
小钱和小鸣同学在实验室里进行的一些化学探究实验,下图是他们进行实验的一些装置图.
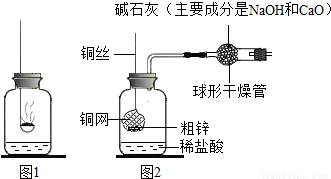
(1)他们利用图1装置探究质量守恒定律的实验,实验过程如下表.
①实验中盐酸与大理石反应后出现橡皮塞被弹出来的情况,其可能的原因是______.
②小钱同学认为实验过程中缺少一个重要步骤,这个步骤是______.
③实验时______(选填“可以”或“不可以”)用硫酸代替盐酸,原因是______.
(2)他们还制作了一套如图2的装置,并用该装置测定粗锌样品的含锌量.
①称量10.0g粗锌放在铜网中,按图将仪器组装好以后,称得仪器和药品总质量为120.0g.②将铜网插人足量稀盐酸中,充分反应,可以观察到的实验现象为______,反应的化学方程式______.
③反应完全后,称得装置总质量为119.8g.则粗锌的纯度为______.
④该实验中碱石灰的作用是______.若不用碱石灰,则所测定的粗锌纯度______(填“偏大”、“偏小”或“无影响”.不考虑空气中C02和H2O对实验的影响).
⑤若将粗锌换成石灰石,原实验方案______(填“能”或“不能”)用于石灰石样品纯度的测定,理由是______.

(1)他们利用图1装置探究质量守恒定律的实验,实验过程如下表.
| 实验过程 | 实验数据记录 |
| 在瓶底放入少量盐酸,将少量大理石粉末放在燃烧匙上,塞紧橡皮塞. | 应记录的实验数据是______. |
| 将燃烧匙上的大理石粉末抖下,使其与盐酸接触. | 应记录的实验数据是______. |
②小钱同学认为实验过程中缺少一个重要步骤,这个步骤是______.
③实验时______(选填“可以”或“不可以”)用硫酸代替盐酸,原因是______.
(2)他们还制作了一套如图2的装置,并用该装置测定粗锌样品的含锌量.
①称量10.0g粗锌放在铜网中,按图将仪器组装好以后,称得仪器和药品总质量为120.0g.②将铜网插人足量稀盐酸中,充分反应,可以观察到的实验现象为______,反应的化学方程式______.
③反应完全后,称得装置总质量为119.8g.则粗锌的纯度为______.
④该实验中碱石灰的作用是______.若不用碱石灰,则所测定的粗锌纯度______(填“偏大”、“偏小”或“无影响”.不考虑空气中C02和H2O对实验的影响).
⑤若将粗锌换成石灰石,原实验方案______(填“能”或“不能”)用于石灰石样品纯度的测定,理由是______.