题目内容
图(Ⅰ)是实验室里测定空气中氧气含量的装置.
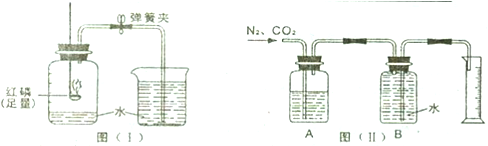
(1)红磷在空气中燃烧的化学方程式为______.
(2)当红磷熄灭并冷却到室温后,打开弹簧夹,看到的现象是______.
(3)如果红磷熄灭后没有完全冷却到室温就打开弹簧夹,实验测定结果会偏低,其原因是______.
(4)上述实验提供了一种粗略测定混合气体中某种气体体积含量的方法.如果要测定氮气、二氧化碳混合气体中二氧化碳的体积量,可将一定体积的混合气体样品通入图(Ⅱ)所示的装置.其中A瓶中装有足量的______溶液,实验结束后,量筒中水的体积约等于______的体积.

(1)红磷在空气中燃烧的化学方程式为______.
(2)当红磷熄灭并冷却到室温后,打开弹簧夹,看到的现象是______.
(3)如果红磷熄灭后没有完全冷却到室温就打开弹簧夹,实验测定结果会偏低,其原因是______.
(4)上述实验提供了一种粗略测定混合气体中某种气体体积含量的方法.如果要测定氮气、二氧化碳混合气体中二氧化碳的体积量,可将一定体积的混合气体样品通入图(Ⅱ)所示的装置.其中A瓶中装有足量的______溶液,实验结束后,量筒中水的体积约等于______的体积.
(1)红磷在氧气中燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2
2P2O5.
(2)待燃烧停止并冷却至室温时打开弹簧夹,由于瓶内气体减少而使压强小于外界大气压,在大气压的作用下,烧杯内的水会沿导管流入瓶内,补充减少的气体所占据的体积,可观察到烧杯中的水沿导管流进集气瓶中,约占集气瓶剩余空间的五分之一.
(3)如果红磷熄灭后没有完全冷却到室温就打开弹簧夹,与室温相比,剩余气体温度较高,压强偏大,因此进入集气瓶中的水会偏少.
(4)粗略测定混合气体中氮气的体积分数,是通过用一氧化碳排出水,测出水的体积,即为氮气的体积,所以要把其中的二氧化碳除掉,用氢氧化钠溶液就能吸收掉.
故答案为:
(1)4P+5O2
2P2O5;
(2)烧杯中的水沿导管流进集气瓶中,约占集气瓶剩余空间的五分之一;
(3)与室温相比,剩余气体温度较高,压强偏大,因此进入集气瓶中的水会偏少;
(4)氢氧化钠;氮气.
| ||
(2)待燃烧停止并冷却至室温时打开弹簧夹,由于瓶内气体减少而使压强小于外界大气压,在大气压的作用下,烧杯内的水会沿导管流入瓶内,补充减少的气体所占据的体积,可观察到烧杯中的水沿导管流进集气瓶中,约占集气瓶剩余空间的五分之一.
(3)如果红磷熄灭后没有完全冷却到室温就打开弹簧夹,与室温相比,剩余气体温度较高,压强偏大,因此进入集气瓶中的水会偏少.
(4)粗略测定混合气体中氮气的体积分数,是通过用一氧化碳排出水,测出水的体积,即为氮气的体积,所以要把其中的二氧化碳除掉,用氢氧化钠溶液就能吸收掉.
故答案为:
(1)4P+5O2
| ||
(2)烧杯中的水沿导管流进集气瓶中,约占集气瓶剩余空间的五分之一;
(3)与室温相比,剩余气体温度较高,压强偏大,因此进入集气瓶中的水会偏少;
(4)氢氧化钠;氮气.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
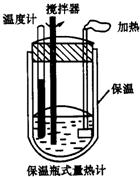 22、小明在爸爸的实验室里看见到如图所示的“保温瓶式量热计”.这种仪器由保温和测温两部分组成的,它不让反应产生的热散失出去,也不让外界的热传递进来,可用于测量化学反应产生的热量.爸爸将不同浓度的酸(A)和碱(B)溶液各100mL在量热计中混合,让小明记录了每次混合前后量热计重温度的升高值△t,得到下表.
22、小明在爸爸的实验室里看见到如图所示的“保温瓶式量热计”.这种仪器由保温和测温两部分组成的,它不让反应产生的热散失出去,也不让外界的热传递进来,可用于测量化学反应产生的热量.爸爸将不同浓度的酸(A)和碱(B)溶液各100mL在量热计中混合,让小明记录了每次混合前后量热计重温度的升高值△t,得到下表.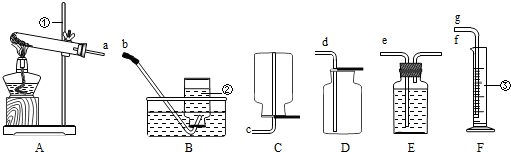
 (2008?厦门)小华为研究养鱼池中水的溶解氧(指水中溶解的氧气,水中溶解氧要4mg?L-1以上鱼才能正常生活),购得如图“溶解氧测试盒”,请你和小华一起研究,并填空:
(2008?厦门)小华为研究养鱼池中水的溶解氧(指水中溶解的氧气,水中溶解氧要4mg?L-1以上鱼才能正常生活),购得如图“溶解氧测试盒”,请你和小华一起研究,并填空: