题目内容
将12g硝酸钾完全溶解在水中,得到溶液的溶质质量分数为12%,则溶剂的质量是________.
88g
分析:溶质质量分数=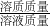 ×100%,可以据此公式的变形来求算出溶液的质量,然后根据溶液质量=溶质质量+溶剂质量求算出溶剂的质量.
×100%,可以据此公式的变形来求算出溶液的质量,然后根据溶液质量=溶质质量+溶剂质量求算出溶剂的质量.
解答:根据溶质质量分数=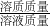 ×100%可以知道,所得溶液质量为:12g÷12%=100g,所以溶剂的质量为:100g-12g=88g.
×100%可以知道,所得溶液质量为:12g÷12%=100g,所以溶剂的质量为:100g-12g=88g.
故答案为88g.
点评:解答这类题目时,首先,要熟记和理解溶质的质量分数及其有关计算方法,有关化学方程式的计算方法,以及质量守恒定律解等相关知识;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,细致地阅读、分析题意等,联系着生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可.
分析:溶质质量分数=
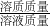 ×100%,可以据此公式的变形来求算出溶液的质量,然后根据溶液质量=溶质质量+溶剂质量求算出溶剂的质量.
×100%,可以据此公式的变形来求算出溶液的质量,然后根据溶液质量=溶质质量+溶剂质量求算出溶剂的质量.解答:根据溶质质量分数=
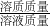 ×100%可以知道,所得溶液质量为:12g÷12%=100g,所以溶剂的质量为:100g-12g=88g.
×100%可以知道,所得溶液质量为:12g÷12%=100g,所以溶剂的质量为:100g-12g=88g.故答案为88g.
点评:解答这类题目时,首先,要熟记和理解溶质的质量分数及其有关计算方法,有关化学方程式的计算方法,以及质量守恒定律解等相关知识;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,细致地阅读、分析题意等,联系着生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可.

练习册系列答案
相关题目
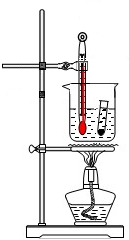 实验装置如图所示,试管中装有水12g及硝酸钾9g,搅拌后试管底部尚有部分未溶的固体.将此试管放入烧杯中隔水加热并摇动试管,当烧杯中的温度达60℃时,试管中的固体恰好完全溶解.若不计加热过程中所蒸发的水量,则有关此试管内溶液的叙述,正确的是( )
实验装置如图所示,试管中装有水12g及硝酸钾9g,搅拌后试管底部尚有部分未溶的固体.将此试管放入烧杯中隔水加热并摇动试管,当烧杯中的温度达60℃时,试管中的固体恰好完全溶解.若不计加热过程中所蒸发的水量,则有关此试管内溶液的叙述,正确的是( )| A、加热前此溶液已达饱和状态 | B、由室温加热至60℃的过程中,此溶液的浓度不变 | C、在60℃时此溶液的质量分数为75% | D、由60℃加热至65℃时此溶液的质量分数不变 |

