题目内容
【题目】某同学在探究久置氢氧化钠固体成分时,进行如下实验,回答相关问题:
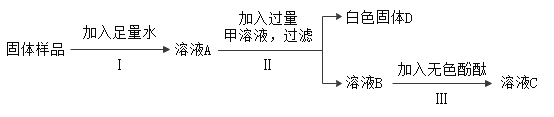
(1)为加速I的进行,可采用的方法为______________(写一种即可)。
(2)以下说法正确的是_______________(填序号)。
①甲溶液可以为稀盐酸或氯化钙溶液(CaCl2溶液呈中性)
②Ⅱ、Ⅲ过程中均有明显现象,说明氢氧化钠部分变质
③溶液B中的溶质为氢氧化钠和甲
(3)II过程中发生反应的化学方程式为_____________(写一个)。
(4)若只进行I、Ⅱ过程,能否验证氢氧化钠部分变质,请解释原因___________。
【答案】使用玻璃棒搅拌(合理即可) ② ![]() (合理即可) 不能,若只进行I、Ⅱ过程,只能检验固体样品中是否含有碳酸钠,确定固体是否变质,无法确定氢氧化钠固体部分变质(合理即可)
(合理即可) 不能,若只进行I、Ⅱ过程,只能检验固体样品中是否含有碳酸钠,确定固体是否变质,无法确定氢氧化钠固体部分变质(合理即可)
【解析】
(1)I过程中固体样品中加入水,使用玻璃棒搅拌可加速固体溶解。
(2) ①甲溶液不能为稀盐酸,可以为氯化钙,因为加入过量的稀盐酸不会产生白色沉淀,且会进入溶液B,而酚酞遇酸不变色,就不能证明原固体样品中是否存在氢氧化钠,故选项错误;
②II中产生白色沉淀,说明原固体样品中存在碳酸钠,Ⅲ中明显现象应是溶液变为红色,说明原固体样品中有氢氧化钠,说明氢氧化钠部分变质,选项正确;
③若氢氧化钠部分变质,溶液B中为氢氧化钠和所加过量的甲,且还有与甲溶液反应生成的氯化钠等钠盐;若氢氧化钠全部变质,则溶液B中的溶质为过量的甲和与甲溶液反应生成的氯化钠等钠盐,③错误;故选:②。
(3) II 过程中若加入的甲为氯化钙溶液,则发生的反应为碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,化学方程式为: ![]() 。
。
(4)若只进行I、Ⅱ过程,只能检验固体样品中是否含有碳酸钠,确定固体是否变质,无法检验样品中是否有氢氧化钠,则无法确定氢氧化钠固体部分变质。

 名校课堂系列答案
名校课堂系列答案【题目】已知某黑色粉末可能是由铁粉、氧化亚铁、四氧化三铁的一种或两种组成,某化学兴趣小组为确定黑色粉末的成分进行了如下探究。
[查阅资料]铁的氧化物均能与稀酸反应,且只有四氧化三铁能被磁铁吸引。
[方案设计]
实验操作 | 实验现象 | 实验结论 |
实验一:取适量的黑色粉末,用磁铁吸引 | ______________。 | 黑色固体粉末中一定不含氧化亚铁 |
实验二:_______________。 | 有气泡产生,溶液颜色发生改变 | 黑色固体一定含有铁粉,可能含有四氧化三铁 |
[交流反思]为探究黑色粉末是否含有四氧化三铁,小明认为可将实验二的操作改为取适量黑色固体粉末于试管中,加入足量的硫酸铜溶液,当出现_____________时,可证明黑色固体粉末中一定含有铁粉和四氧化三铁。
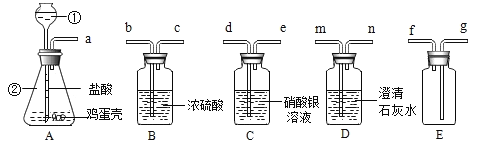
[继续探究]为探究黑色粉末成分中铁粉和四氧化三铁的质量比,同学进行了如图实验;反应前称取10g黑色粉末加入玻璃管内(玻璃管的质量为50 g) ,先通入一段时间一氧化碳气体,然后点燃酒精灯。
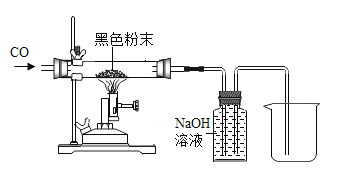
(1)反应前先通入一氧化碳气体再点燃酒精灯,目的是______________。
(2)充分反应后熄灭酒精灯,继续通入一氧化碳,待冷却到室温后停止通入,称量玻璃管和管内固体总质量为58.4g,计算黑色粉末中铁和四氧化三铁的质量比为___________________。
(3)虚线框内的装置的作用是_________________。