题目内容
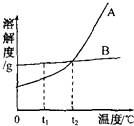
【题目】下图是KNO3和NaCl的溶解度曲线。下列说法中正确的是( )
A.NaCl的溶解度大于KNO3的溶解度
B.在温度高于t2℃时,100gKNO3饱和溶液中溶质的质量大于100g NaCl饱和溶液中溶质的质量
C.t1℃时,KNO3饱和溶液中溶质的质量分数是20%
D.t2℃时的NaCl溶液与KNO3溶液中,溶质的质量分数相等
【答案】B
【解析】由题中信息知,A. t2℃前 NaCl的溶解度大于KNO3的溶解度;t2℃后反而小于。故A错误。B. 在温度高于t2℃时,100gKNO3饱和溶液中溶质的质量大于100g NaCl饱和溶液中溶质的质量。KNO3溶解度大于NaCl溶解度。故B正确。C. t1℃时,KNO3饱和溶液中溶质的质量分数是 ![]() ×100%=16.7%.故C错误。D. t2℃时的NaCl饱和溶液与饱和KNO3溶液中,溶质的质量分数相等。故D错误。
×100%=16.7%.故C错误。D. t2℃时的NaCl饱和溶液与饱和KNO3溶液中,溶质的质量分数相等。故D错误。
【考点精析】利用固体溶解度曲线及其作用和溶质的质量分数、溶解性和溶解度的关系对题目进行判断即可得到答案,需要熟知1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和);溶质质量分数 =溶质质量/溶液质量*100% ;溶解度=溶质质量/溶剂质量*100g (必须选取饱和溶液);溶液质量=溶质质量(克)+溶剂质量(克) ;对于饱和溶液,溶液质量分数w = S/(S+100);所以溶解度S = 100/(1/w-1).

练习册系列答案
相关题目