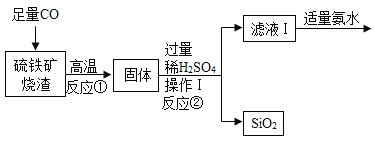
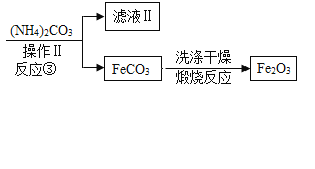
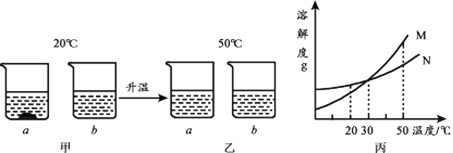
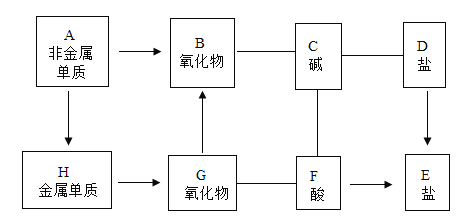
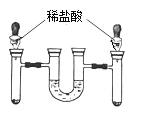
题目内容
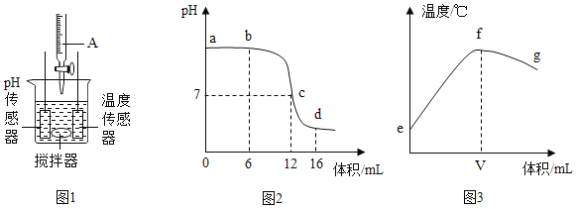
【题目】实验室有一份在空气中潮解部分变质的氢氧化钠样品,质量为1.86g。某实验小组将这份样品完全溶解,配成 50g 溶液,然后缓慢滴入 7.3%的稀盐酸,同时进行搅拌,使二氧化碳全部逸出。滴加过程中,多次测得溶液 pH 和溶液总质量,部分数据如下表所示:
测量次数 | 第 1 次 | 第 2 次 | 第 3 次 | 第 4 次 | 第 5 次 |
滴加的盐酸总质量/g | 0 | 5 | 20 | 30 | 35 |
溶液总质量/g | 50 | 55 | 69.56 | 79.56 | 84.56 |
溶液 pH | 12.4 | 12.1 | 7.0 | 2.2 | 2.1 |
请分析计算:
(1)氢氧化钠变质是与空气中的_________________反应。
(2)实验中生成二氧化碳的质量为___________________g。
(3)求样品中氢氧化钠的质量___________________。
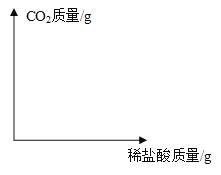
(4)请在下图中画出稀盐酸质量与二氧化碳质量关系的图像___________________(温馨提醒:标出关键点的数据)。
(5)当恰好完全反应时,该溶液的溶质质量分数是_________。(结果保留一位小数)。
【答案】二氧化碳 0.44 0.8  0.34%
0.34%
【解析】
(1)氢氧化钠与空气中的二氧化碳反应生成碳酸钠和水而变质;
(2)生成二氧化碳的质量为50g+20g-69.56g=0.44g;
(3)设生成0.44g二氧化碳需要碳酸钠的质量为x,与碳酸钠反应的氯化氢的质量为y,

![]() x=1.06g,
x=1.06g,
![]() y=0.73g,
y=0.73g,
样品中氢氧化钠的质量=1.86g-1.06g=0.8g;
(4)与碳酸钠反应的盐酸的质量:0.73g![]() 7.3%=10g,根据第3次实验时pH=7,表示恰好完全反应;根据第3次实验时pH=7,表示恰好完全反应,则与氢氧化钠反应的盐酸的质量:20g-10g=10g,所以稀盐酸质量与二氧化碳质量关系,如图:
7.3%=10g,根据第3次实验时pH=7,表示恰好完全反应;根据第3次实验时pH=7,表示恰好完全反应,则与氢氧化钠反应的盐酸的质量:20g-10g=10g,所以稀盐酸质量与二氧化碳质量关系,如图: ;
;
(5)设恰好完全反应时,生成氯化钠的质量为m,则:
根据Na2CO3+2HCl═2NaCl+H2O+CO2↑、NaOH+HCl=NaCl+H2O可得:
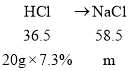
![]() m=0.234g,
m=0.234g,
当恰好完全反应时,该溶液的溶质质量分数是![]() 。
。

【题目】下列图像不能正确反映对应变化关系的是
|
|
|
|
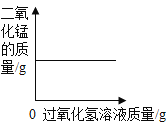
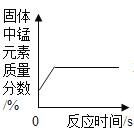
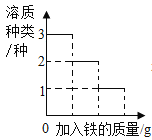
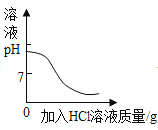
A向一定量的二氧化锰中加入过氧化氢溶液 | B加热一定量的高锰酸钾固体 | C在一定量 AgNO3和 Cu(NO3)2 的混合溶液中加入铁粉 | D向 NaOH 溶液中滴加稀盐酸至过量 |
A.AB.BC.CD.D
【题目】分类、类比是学习化学常用的方法。
(1)初中化学实验方法有多种,如对比法、控制变量法、定量实验法、定性实验法等,若按实验方法分类,应将实验 ________________________(填字母)分为一类,依据是______________________________。
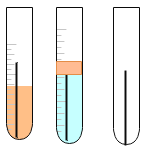
用pH 试纸测定溶液的pH |
探究铁生锈条件 |
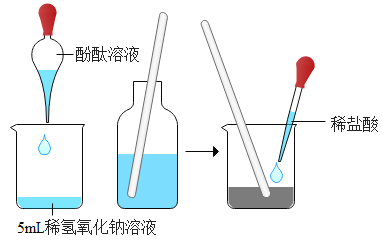
探究氢氧化钠溶液与盐酸反应 |
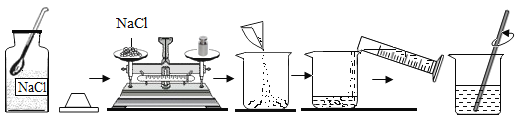
配置质量分数5%的NaCl 溶液 |
A | B | C | D |
(2)善于比较、归纳是良好的学习习惯。酸酐能与水化合生成相应的酸。依据酸酐中元素的化合价与酸中元素的化合价存在的规律,写出硝酸酸酐的化学式__________________;请写出三氧化二氮与水反应生成相应酸的化学方程式_______________________。
酸酐 | 酸 | 酸酐 | 酸 |
CO2 | H2CO3 | SO3 | H2SO4 |
Cl2O7 | HClO4 | ? | HNO3 |