题目内容
赤铁矿(主要成分是Fe2O3)是我国铁矿石资源中的一种.请计算:(1)Fe2O3中Fe元素的质量分数是
(2)
分析:(1)根据物质氧化铁的化学式,利用元素的相对原子质量进行组成元素质量分数的计算;
(2)根据铁元素质量守恒进行计算;
(2)根据铁元素质量守恒进行计算;
解答:解:(1)氧化铁中铁元素的质量分数=
×100%=70%;
(2)据题意Fe2O3的质量应为:
=8kg.
故答案为:70%、8kg.
| 56×2 |
| 56×2+16×3 |
(2)据题意Fe2O3的质量应为:
| 5.6kg |
| 70% |
故答案为:70%、8kg.
点评:根据物质的化学式,利用元素的相对原子质量进行组成元素质量分数的计算是解决问题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

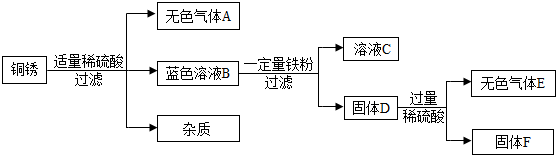

 (2013?兰州)已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫色金属;H是蓝色沉淀.根据图示的转化关系(图中反应条件均已略去),请回答:
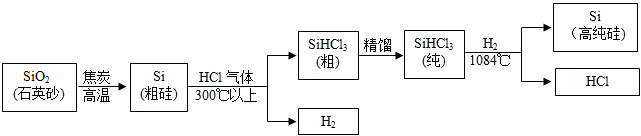
(2013?兰州)已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫色金属;H是蓝色沉淀.根据图示的转化关系(图中反应条件均已略去),请回答: A-F和X都是初中化学中的常见物质,其中A、C是无色气体,B是赤铁矿的主要成分,F是红色固体,其中只有D、F为单质,X为蓝色溶液,它们的转化关系如图所示(部分生成物已省略):
A-F和X都是初中化学中的常见物质,其中A、C是无色气体,B是赤铁矿的主要成分,F是红色固体,其中只有D、F为单质,X为蓝色溶液,它们的转化关系如图所示(部分生成物已省略): 已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫色金属;H是蓝色沉淀.根据图示的转化关系(图中反应条件均已略去),请回答:
已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫色金属;H是蓝色沉淀.根据图示的转化关系(图中反应条件均已略去),请回答: