题目内容
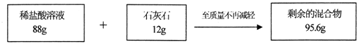
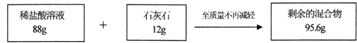
我市某校九年级学生去云龙山春游,带回几块石灰石样品,为测定石灰石中碳酸钙的质量分数,实验测得相关数据如图所示:(假设其他物质不与盐酸反应)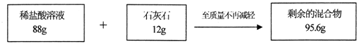
(1)反应生成二氧化碳的质量为______g.
(2)计算石灰石中碳酸钙的质量分数.(写出计算过程)
【答案】分析:(1)根据质量守恒定律分析可知减少的质量即为生成的二氧化碳的质量;
(2)根据方程式,依据生成二氧化碳的质量求出参与反应的碳酸钙的质量;从而求出碳酸钙的质量分数
解答:解:(1)根据质量守恒定律分析可知减少的质量即为生成的二氧化碳的质量,即为:88g+12g-95.6g=4.4g
(2)设石灰石中碳酸钙的质量为x;
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
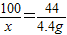
x=10g
石灰石中碳酸钙质量分数为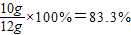
答:石灰石中碳酸钙的质量分数为83.3%
故答案为:(1)4.4(2)83.3%
点评:本题主要考查根据化学方程式的基本计算,考查学生运用所学化学知识分析和解决实际问题的能力
(2)根据方程式,依据生成二氧化碳的质量求出参与反应的碳酸钙的质量;从而求出碳酸钙的质量分数
解答:解:(1)根据质量守恒定律分析可知减少的质量即为生成的二氧化碳的质量,即为:88g+12g-95.6g=4.4g
(2)设石灰石中碳酸钙的质量为x;
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
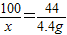
x=10g
石灰石中碳酸钙质量分数为
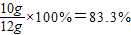
答:石灰石中碳酸钙的质量分数为83.3%
故答案为:(1)4.4(2)83.3%
点评:本题主要考查根据化学方程式的基本计算,考查学生运用所学化学知识分析和解决实际问题的能力

练习册系列答案
相关题目