题目内容
(9分)从C、H、O、N、S、P、Na、Fe、Ba等9种元素中选择恰当的元素,用离子符号、化学式或化学方程式按下列要求填空:
(1)硫酸钠中的阴离子 ;氯化亚铁中的阳离子 ;能使木材、纸张变黑的酸 ;溶于水后显碱性的气体 ;用于造纸、洗涤剂的盐 。
(2)一种暗红色的固体燃烧生成大量的白烟 。
(3)高炉炼铁(以赤铁矿为例)过程中还原成铁的主要反应原理 。
(4)有沉淀生成的中和反应 。
(5)在人体组织里,葡萄糖在酶的作用下发生缓慢氧化 。
(1)硫酸钠中的阴离子 ;氯化亚铁中的阳离子 ;能使木材、纸张变黑的酸 ;溶于水后显碱性的气体 ;用于造纸、洗涤剂的盐 。
(2)一种暗红色的固体燃烧生成大量的白烟 。
(3)高炉炼铁(以赤铁矿为例)过程中还原成铁的主要反应原理 。
(4)有沉淀生成的中和反应 。
(5)在人体组织里,葡萄糖在酶的作用下发生缓慢氧化 。
(1)SO42-; Fe2+; 浓H2SO4; NH3; Na2CO3
(2)4P+5O2 2P2O5 (3)3CO+Fe2O3
2P2O5 (3)3CO+Fe2O3 2Fe+3CO2
2Fe+3CO2
(4)H2SO4+Ba(OH)2 BaSO4↓+2H2O (5)C6H12O6 + 6O2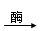 6CO2+6H2O
6CO2+6H2O
(2)4P+5O2
 2P2O5 (3)3CO+Fe2O3
2P2O5 (3)3CO+Fe2O3 2Fe+3CO2
2Fe+3CO2 (4)H2SO4+Ba(OH)2 BaSO4↓+2H2O (5)C6H12O6 + 6O2
 6CO2+6H2O
6CO2+6H2O 试题分析:(1)硫酸钠中的阴离子SO42-;氯化亚铁中的阳离子Fe2+;能使木材、纸张变黑的酸浓H2SO4;溶于水后显碱性的气体NH3;用于造纸、洗涤剂的盐Na2CO3;
(2)一种暗红色的固体燃烧生成大量的白烟,是红磷燃烧,化学方程式为4P+5O2
 2P2O5;
2P2O5;(3)高炉炼铁(以赤铁矿为例)过程中还原成铁的主要反应原理是:3CO+Fe2O3
 2Fe+3CO2;
2Fe+3CO2;(4)有沉淀生成的中和反应是H2SO4+Ba(OH)2 BaSO4 ↓+2H2O;
(5)在人体组织里,葡萄糖在酶的作用下发生缓慢氧化,表达式为:C6H12O6 + 6O2
 6CO2+6H2O。
6CO2+6H2O。点评:浓硫酸具有脱水性,可以使木材、纸张变黑;红磷燃烧生成大量的白烟;酸和碱作用,生成盐和水电额反应时中和反应;书写化学方程式要遵循客观事实和质量守恒定律两个原则,注意化学式要正确,不要忘记反应条件、气体或者沉淀符号。

练习册系列答案
相关题目
