题目内容
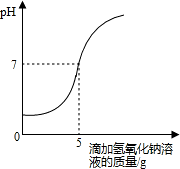 硫酸厂排放的污水中通常含有硫酸杂质.为测定污水中硫酸的溶质质量分数做如下实验:取10g该污水,向污水中逐滴加入溶质质量分数为4%的氢氧化钠溶液,所滴加氢氧化钠溶液的质量与溶液pH变化关系如图所示.请根据实验计算,该污水中硫酸的溶质质量分数是多少?
硫酸厂排放的污水中通常含有硫酸杂质.为测定污水中硫酸的溶质质量分数做如下实验:取10g该污水,向污水中逐滴加入溶质质量分数为4%的氢氧化钠溶液,所滴加氢氧化钠溶液的质量与溶液pH变化关系如图所示.请根据实验计算,该污水中硫酸的溶质质量分数是多少?
解:设样品中H2SO4的质量为x,
2NaOH+H2SO4=Na2SO4+2H2O
80 98
5g×4%,x
∴ ,
,
解之得:x=0.245g,
则该污水中硫酸的溶质质量分数是: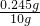 ×100%=2.45%.
×100%=2.45%.
答:该污水中硫酸的溶质质量分数是2.45%.
分析:已知中性溶液的ph值为7,由图示数据可知,向污水中滴加氢氧化钠溶液至5g时,与硫酸完全反应.利用氢氧化钠与硫酸反应的化学方程式和氢氧化钠的质量,列出比例式,可计算出样品中H2SO4的质量;然后根据溶质质量分数公式计算即可.
点评:本题是有关化学方程式和溶质质量分数的简单计算.解题时要注意格式和步骤.
2NaOH+H2SO4=Na2SO4+2H2O
80 98
5g×4%,x
∴
 ,
,解之得:x=0.245g,
则该污水中硫酸的溶质质量分数是:
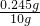 ×100%=2.45%.
×100%=2.45%.答:该污水中硫酸的溶质质量分数是2.45%.
分析:已知中性溶液的ph值为7,由图示数据可知,向污水中滴加氢氧化钠溶液至5g时,与硫酸完全反应.利用氢氧化钠与硫酸反应的化学方程式和氢氧化钠的质量,列出比例式,可计算出样品中H2SO4的质量;然后根据溶质质量分数公式计算即可.
点评:本题是有关化学方程式和溶质质量分数的简单计算.解题时要注意格式和步骤.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
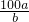 g
g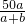 %,则x=2b
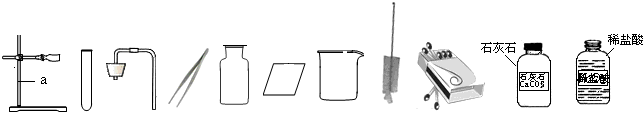
%,则x=2b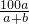 %
%
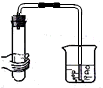 Ⅱ.加入药品
Ⅱ.加入药品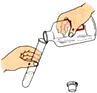 Ⅲ.收集气体
Ⅲ.收集气体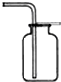 Ⅳ.气体验满
Ⅳ.气体验满 Ⅴ.洗涤仪器,整理表面
Ⅴ.洗涤仪器,整理表面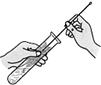
 为纪念化学学科所取得的成就以及对人类文明的贡献,联合国将2011年定为“国际化学年”.下列对化学学科的认识中错误的是
为纪念化学学科所取得的成就以及对人类文明的贡献,联合国将2011年定为“国际化学年”.下列对化学学科的认识中错误的是