题目内容
(7分)溶液的微粒构成决定其性质,溶液的宏观组成是其成分计算的依据。
(1)氯化钠晶体是由 (填微粒符号)构成的。氯化钠溶于水,溶液导电能力显著增强,是因为其溶液中含有 ;而蔗糖溶于水,溶液很难导电,是因为 的缘故。
(2)用溶质质量分数为15%的氯化钠溶液来配制500g溶质质量分数为6%的氯化钠溶液,
需要15%的氯化钠溶液 g。
(3)某温度下饱和氯化钠溶液的溶质质量分数为26%,试列式计算该温度下氯化钠的溶解度S(计算结果保留小数点后一位)。
(1)氯化钠晶体是由 (填微粒符号)构成的。氯化钠溶于水,溶液导电能力显著增强,是因为其溶液中含有 ;而蔗糖溶于水,溶液很难导电,是因为 的缘故。
(2)用溶质质量分数为15%的氯化钠溶液来配制500g溶质质量分数为6%的氯化钠溶液,
需要15%的氯化钠溶液 g。
(3)某温度下饱和氯化钠溶液的溶质质量分数为26%,试列式计算该温度下氯化钠的溶解度S(计算结果保留小数点后一位)。
(1)Na+、Cl-;自由移动的钠离子Na+和氯离子Cl-;蔗糖不电离,溶液中没有自由移动的带电微粒;(2)200g;(3)35.1g
试题分析:(1)氯化钠晶体是由钠离子Na+和氯离子Cl-构成的。氯化钠溶于水,溶液导电能力显著增强,是因为其溶液中含有自由移动的钠离子Na+和氯离子Cl-;而蔗糖溶于水,溶液很难导电,是因为 蔗糖不电离,没有自由移动的带电微粒;(2)溶液稀释前后溶质质量不变;设需要用溶质质量分数为15%的氯化钠溶液来的质量为x,则15%x="500g×" 6% x=;(3)某温度下饱和氯化钠溶液的溶质质量分数为26%,,利用饱和溶液的溶质质量分数=
 ×100%=
×100%=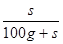 ×100%=26%。解得s≈35.1g
×100%=26%。解得s≈35.1g
练习册系列答案
相关题目