题目内容
(2011?杨浦区一模)以下是气体制取与性质验证的组合实验.如果打开分液漏斗活塞后,A中出现大量气泡,B中白磷燃烧,C中液面下降,稀盐酸逐渐进入D中.
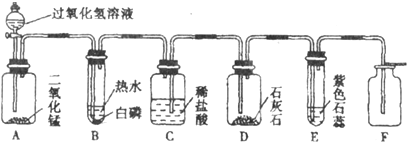
请看图回答问题:
(1)B中白磷能够燃烧的原因是
(2)A装置中盛放过氧化氢溶液的仪器名称
(3)E中的实验现象是
(4)用F装置收集气体的依据是

请看图回答问题:
(1)B中白磷能够燃烧的原因是
与氧气接触,温度达到着火点
与氧气接触,温度达到着火点
.(2)A装置中盛放过氧化氢溶液的仪器名称
分液漏斗
分液漏斗
,此装置中MnO2的作用是催化
催化
,A、B中发生反应的化学方程式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
、
| ||
4P+5O2
2P2O5
| ||
4P+5O2
2P2O5
、
| ||
(3)E中的实验现象是
溶液由紫色变红色
溶液由紫色变红色
,说明溶液呈酸
酸
性,请用化学方程式表示其原因H2O+CO2═H2CO3
H2O+CO2═H2CO3
.(4)用F装置收集气体的依据是
气体的密度比空气密度大
气体的密度比空气密度大
.分析:根据已有的知识进行分析,可燃物燃烧需要与氧气接触且温度达到其着火点,使用过氧化氢制取氧气时,需要加入二氧化锰,此时二氧化锰起催化作用,磷燃烧能生成五氧化二磷,二氧化碳能与水反应生成碳酸,碳酸呈酸性,使用向上排空气法收集的气体需要具备密度比空气大的性质.
解答:解:(1)白磷能够燃烧说明白磷与氧气接触且温度达到了其着火点,故填:与氧气接触,温度达到着火点;
(2)据图可知,盛过氧化氢的仪器是分液漏斗,二氧化锰起催化作用,过氧化氢在二氧化锰的催化作用下生成水喝氧气,磷燃烧能生成水喝氧气,故填:分液漏斗,催化,2H2O2
2H2O+O2↑,4P+5O2
2P2O5;
(3)碳酸钙与盐酸反应生成的二氧化碳能与水反应生成碳酸,碳酸呈酸性,能使石蕊试液变红,故填:溶液由紫色变红色,酸,H2O+CO2═H2CO3;
(4)使用向上排空气法收集的气体需要具备密度比空气大的性质,故填:气体的密度比空气密度大.
(2)据图可知,盛过氧化氢的仪器是分液漏斗,二氧化锰起催化作用,过氧化氢在二氧化锰的催化作用下生成水喝氧气,磷燃烧能生成水喝氧气,故填:分液漏斗,催化,2H2O2
| ||
| ||
(3)碳酸钙与盐酸反应生成的二氧化碳能与水反应生成碳酸,碳酸呈酸性,能使石蕊试液变红,故填:溶液由紫色变红色,酸,H2O+CO2═H2CO3;
(4)使用向上排空气法收集的气体需要具备密度比空气大的性质,故填:气体的密度比空气密度大.
点评:本题考查了实验室制取氧气的知识,完成此题,可以依据已有的知识进行,要求同学们加强对基本实验的掌握,以便灵活应用.

练习册系列答案
相关题目
