题目内容
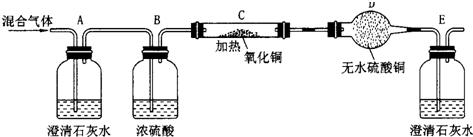
有一气体可能是CO、CO2、H2、HCl气体的混合物,依次通过如下装置:
现象如下:A中石灰水不浑浊,C中黑色粉末变红,D中无水硫酸铜不变色,E中石灰水变浑浊,假设每一步中气体均反应完全,试推断:混合气体中一定存在______,一定不存在______,可能存在______或______.
【答案】分析:通过分析现象回答问题:通过澄清石灰水变浑浊说明有二氧化碳,通过灼热氧化铜黑色粉末变红说明具有还原性气体,无水硫酸铜白色粉末变蓝说明有水生成.要注意二氧化碳和氯化氢的混合气体不能使澄清的石灰水变浑浊,还要注意气体在因发生反应被除去的同时是否又生成了新气体.
解答:解:通过澄清的石灰水时无沉淀,说明原气体中无二氧化碳或同时含有二氧化碳和氯化氢,通过灼热的氧化铜,黑色粉末变红但无水出现,说明原气体中有一氧化碳且无氢气.将剩余气体通过澄清石灰水时,有白色沉淀生成,进一步说明原气体中有一氧化碳.
故答案为:CO;H2;HCl; CO2 和HCl
点评:掌握几种气体的化学性质是解题的前提,同时要认真分析现象出现的真正原因,要排除干扰,想到所有细节.
解答:解:通过澄清的石灰水时无沉淀,说明原气体中无二氧化碳或同时含有二氧化碳和氯化氢,通过灼热的氧化铜,黑色粉末变红但无水出现,说明原气体中有一氧化碳且无氢气.将剩余气体通过澄清石灰水时,有白色沉淀生成,进一步说明原气体中有一氧化碳.
故答案为:CO;H2;HCl; CO2 和HCl
点评:掌握几种气体的化学性质是解题的前提,同时要认真分析现象出现的真正原因,要排除干扰,想到所有细节.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目