题目内容
 30、a、b两物质的溶解度曲线如图1所示,根据图回答:
30、a、b两物质的溶解度曲线如图1所示,根据图回答:(1)a的溶解度为40g时溶液的温度为
30
℃.(2)a的溶解度小于b的溶解度的温度范围是
0~20℃
.(3)10℃时,将a和b两种固体各25g分别加入100 g水中.则a溶液的溶质质量分数
小于
_b溶液的溶质质量分数(填写:大于、等于、小于).(4)如图2所示,现有20℃时等质量的a、b两物质的饱和溶液,分别盛入两只试管中且试管底部有等质量的固体a、b剩余,向烧杯的水中加入氢氧化钠固体,则对相关变化判断正确的是
CD
(不考虑溶剂的蒸发,析出的固体不含水)A.a和b两溶液的质量相等
B.b溶液将由饱和变成不饱和
C.a溶液中溶剂质量等于b溶液中溶剂质量
D.变化后a溶液中溶质质量分数大于b溶液中溶质质量分数
分析:(1)利用溶解度曲线图,查出指定溶解度所对应的温度;
(2)比较两物质的溶解度大小关系,以交点为界,两物质的溶解度大小关系相反;
(3)根据溶解度判断两物质的溶解情况:a物质10℃溶解度较小不能完全溶解,而b物质可以完全溶解;
(4)20℃时a、b两物质的溶解度相等,则此时a、b两物质的饱和溶液的溶质质量分数相同;氢氧化钠固体溶于水放出大量的热使溶液温度升高;b物质溶解度随温度升高而减小,升温b的饱和溶液析出b.
(2)比较两物质的溶解度大小关系,以交点为界,两物质的溶解度大小关系相反;
(3)根据溶解度判断两物质的溶解情况:a物质10℃溶解度较小不能完全溶解,而b物质可以完全溶解;
(4)20℃时a、b两物质的溶解度相等,则此时a、b两物质的饱和溶液的溶质质量分数相同;氢氧化钠固体溶于水放出大量的热使溶液温度升高;b物质溶解度随温度升高而减小,升温b的饱和溶液析出b.
解答:解:(1)根据a物质的溶解度曲线图,可查到30℃该物质的溶解度为40g.
故答:30℃;
(2)a的溶解度小于b的溶解度,即曲线b处于曲线a上方,从0℃到20℃这个范围内都是曲线b处于曲线a上方.
故答:0℃~20℃;
(3)10℃时,将a和b两种固体各25g分别加入100 g水中,根据溶解度曲线可知,25g物质a未全部溶解,25g物质b全部溶解,所以物质a的溶液的溶质质量分数小于物质b的溶液的溶质质量分数.
故答:小于;
(4)A、温度升高,a物质的饱和溶液继续溶解该物质,溶液质量增加;b物质的饱和溶液析出晶体,溶液质量减小.判断错误;
B、温度升高,b物质的饱和溶液析出晶体,析出晶体的溶液仍为饷饱和溶液.判断错误;
C、温度升高,a物质的饱和溶液继续溶解该物质,溶剂质量不变仍为100g;b物质的饱和溶液析出晶体,溶剂质量不变仍为100g.判断正确;
D、温度升高,a物质的饱和溶液继续溶解该物质,溶液的溶质质量分数增加;b物质的饱和溶液析出晶体,溶液的溶质质量分数变小.升温前,20℃时a、b两物质的饱和溶液的溶质质量分数相等.据此可得,升温后a溶液中溶质质量分数大于b溶液中溶质质量分数的判断正确.
故选CD(少选或错选都不给分).
故答:30℃;
(2)a的溶解度小于b的溶解度,即曲线b处于曲线a上方,从0℃到20℃这个范围内都是曲线b处于曲线a上方.
故答:0℃~20℃;
(3)10℃时,将a和b两种固体各25g分别加入100 g水中,根据溶解度曲线可知,25g物质a未全部溶解,25g物质b全部溶解,所以物质a的溶液的溶质质量分数小于物质b的溶液的溶质质量分数.
故答:小于;
(4)A、温度升高,a物质的饱和溶液继续溶解该物质,溶液质量增加;b物质的饱和溶液析出晶体,溶液质量减小.判断错误;
B、温度升高,b物质的饱和溶液析出晶体,析出晶体的溶液仍为饷饱和溶液.判断错误;
C、温度升高,a物质的饱和溶液继续溶解该物质,溶剂质量不变仍为100g;b物质的饱和溶液析出晶体,溶剂质量不变仍为100g.判断正确;
D、温度升高,a物质的饱和溶液继续溶解该物质,溶液的溶质质量分数增加;b物质的饱和溶液析出晶体,溶液的溶质质量分数变小.升温前,20℃时a、b两物质的饱和溶液的溶质质量分数相等.据此可得,升温后a溶液中溶质质量分数大于b溶液中溶质质量分数的判断正确.
故选CD(少选或错选都不给分).
点评:固体物质与水混合放出大量热的有氢氧化钠和氧化钙;与水混合吸收热的固体物质为硝酸铵.这些物质与水混合相当于对溶液升温或降温.

练习册系列答案
相关题目
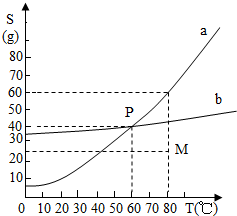 如如图所示为a、b两物质的溶解度曲线,下列根据如图所示中M点和P点,得到的正确信息是( )
如如图所示为a、b两物质的溶解度曲线,下列根据如图所示中M点和P点,得到的正确信息是( )| A、60℃时,a、b两物质饱和溶液的质量分数都为40% | B、80℃时,100g水中溶解25g的a的物质,溶液不饱和 | C、80℃时,将a、b两物质的饱和溶液降温到20℃时,只有a物质析出 | D、向M点的任意量a溶液中,加入(60-25)g溶质,溶液一定达到饱和 |
 25、如图为a、b、c三种物质的溶解度曲线.
25、如图为a、b、c三种物质的溶解度曲线.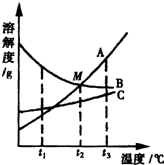 25、A、B、C三种物质的溶解度曲线如右图所示,请回答:
25、A、B、C三种物质的溶解度曲线如右图所示,请回答: (2012?集美区质检)如图是A、B两种固体物质的溶解度随温度变化的曲线.请回答:
(2012?集美区质检)如图是A、B两种固体物质的溶解度随温度变化的曲线.请回答: