题目内容
(1)已知某温度下,A物质(不含结晶水)的溶解度为mg,在此温度下,将agA加入到bg水中,充分搅拌,所得到的溶液的质量分数为 或 ;(2)已知金属钠与水反应的化学方程式为:2Na+2H2O=2NaOH+H2↑,如果将4.6g金属钠投入到95.6g水中,所得溶液的质量分数为 .
【答案】分析:(1)根据饱和溶液概念及溶质质量分数的计算方法分析即可;
(2)根据溶质质量分数的计算方法并结合钠与水的反应原理分析即可.
解答:解:(1)在此温度下,将agA加入到bg水中,不能确定溶液是否饱和,有以下两种情况:
第一种:溶液饱和,所得溶液的溶质质量分数=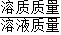 ×100%=
×100%=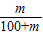 ;
;
第二种:溶液未达到饱和,所得溶液的溶质质量分数=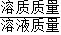 ×100%=
×100%=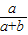 ;
;
故答案为: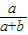 、
、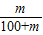 ;
;
(2)解:设4.6g钠与水反应能生成氢氧化钠和氢气的质量分别为x和y则
2Na+2H2O=2NaOH+H2↑
46 80 2
4.6 x y
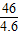 =
=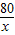 =
=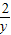
解得x=8 y=0.2
钠溶于水中后溶质是氢氧化钠,溶液的质量=4.6+95.6-0.2=100
所以溶质质量分数=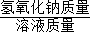 ×100%=
×100%=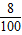 ×100%=8%
×100%=8%
故答案为:8%
点评:若一种物质会与水反应,当把一定量的该物质溶于水后形成的溶液已不是该物质的溶液,而是新生成的物质的溶液;计算溶液的质量时用质量守恒法会很简便,但要注意是否有气体或沉淀从溶液中分离出去.
(2)根据溶质质量分数的计算方法并结合钠与水的反应原理分析即可.
解答:解:(1)在此温度下,将agA加入到bg水中,不能确定溶液是否饱和,有以下两种情况:
第一种:溶液饱和,所得溶液的溶质质量分数=
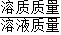 ×100%=
×100%=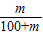 ;
;第二种:溶液未达到饱和,所得溶液的溶质质量分数=
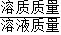 ×100%=
×100%=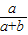 ;
;故答案为:
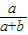 、
、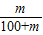 ;
;(2)解:设4.6g钠与水反应能生成氢氧化钠和氢气的质量分别为x和y则
2Na+2H2O=2NaOH+H2↑
46 80 2
4.6 x y
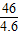 =
=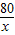 =
=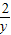
解得x=8 y=0.2
钠溶于水中后溶质是氢氧化钠,溶液的质量=4.6+95.6-0.2=100
所以溶质质量分数=
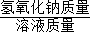 ×100%=
×100%=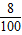 ×100%=8%
×100%=8%故答案为:8%
点评:若一种物质会与水反应,当把一定量的该物质溶于水后形成的溶液已不是该物质的溶液,而是新生成的物质的溶液;计算溶液的质量时用质量守恒法会很简便,但要注意是否有气体或沉淀从溶液中分离出去.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目