题目内容
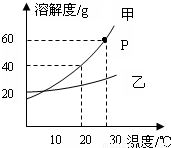
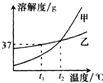
(1)如图是甲、乙两种固体物质的溶解度曲线.①P点的含义是______.
②当甲中含有少量乙时,可采用______的方法提纯甲.
③30℃时,将40g甲物质放入盛有50g水的烧杯中,所得溶液溶质的质量分数为______;若将烧杯内物质升温到50℃(不考虑水蒸发),溶液中变化的是______(填字母).
A.溶剂的质量 B.溶液的质量 C.溶质的质量分数
(2)硫酸钠在不同温度下的溶解度如下表所示:
| 温度/℃ | 10 | 20 | 30 | 40 | |
| 硫酸钠溶解度/g | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 |
【答案】分析:(1)根据固体物质的溶解度曲线意义分析.溶解度曲线上的各点表示该物质在不同温度下的溶解度,可以根据溶解度进行有关的计算;可以看出物质的溶解度受温度变化的影响大小,从而可以判断出提纯物质的方法等;
(2)根据硫酸钠在不同温度下的溶解度及溶解度的意义,分析析出晶体的质量.
解答:解:(1)由溶解度曲线的意义可知,P点的意义是:在30℃时,甲物质的溶解度是60g;
(2)由甲、乙的溶解度曲线的意义可知,甲物质的溶解度随温度的升高而增大;乙物质的溶解度随温度的升高变化不大,当甲中含有少量乙时,可采用冷却热饱和溶液的方法提纯甲;
(3)由甲物质的溶解度曲线的意义可知,在30℃时,甲物质的溶解度是60g.由溶解度的定义可知,30℃时,将40g甲物质放入盛有50g水的烧杯中,只能溶解30g,所得的溶液为饱和溶液,所得溶液溶质的质量分数为: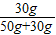
×100%=37.5%;由于甲物质的溶解度随温度的升高而增大,所以,若将烧杯内物质升温到50℃时,未溶解的甲物质又能溶解,所以,溶液的质量增加,溶质的质量分数增大;
(2)由硫酸钠在不同温度下的溶解度表可知,在40℃时,硫酸钠的溶解度是48.4g,在10℃时,硫酸钠的溶解度是9.6g,由溶解度的意义可知,在40℃时,在100g的水中溶解了48.4g硫酸钠,在降温到10℃时,在100g水中只能溶解9.6g.所以析出晶体的质量为:48.4g-9.6g=38.8g.
故答为:(1)①在30℃时,甲物质的溶解度是60g;②冷却热饱和溶液;③B、C;(2)38.8g.
点评:本题是对溶液知识的考查,重点是抓住溶解度的实质,只要结合图表所提供的信息,分项探讨即可解决.
(2)根据硫酸钠在不同温度下的溶解度及溶解度的意义,分析析出晶体的质量.
解答:解:(1)由溶解度曲线的意义可知,P点的意义是:在30℃时,甲物质的溶解度是60g;
(2)由甲、乙的溶解度曲线的意义可知,甲物质的溶解度随温度的升高而增大;乙物质的溶解度随温度的升高变化不大,当甲中含有少量乙时,可采用冷却热饱和溶液的方法提纯甲;
(3)由甲物质的溶解度曲线的意义可知,在30℃时,甲物质的溶解度是60g.由溶解度的定义可知,30℃时,将40g甲物质放入盛有50g水的烧杯中,只能溶解30g,所得的溶液为饱和溶液,所得溶液溶质的质量分数为:
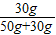
×100%=37.5%;由于甲物质的溶解度随温度的升高而增大,所以,若将烧杯内物质升温到50℃时,未溶解的甲物质又能溶解,所以,溶液的质量增加,溶质的质量分数增大;
(2)由硫酸钠在不同温度下的溶解度表可知,在40℃时,硫酸钠的溶解度是48.4g,在10℃时,硫酸钠的溶解度是9.6g,由溶解度的意义可知,在40℃时,在100g的水中溶解了48.4g硫酸钠,在降温到10℃时,在100g水中只能溶解9.6g.所以析出晶体的质量为:48.4g-9.6g=38.8g.
故答为:(1)①在30℃时,甲物质的溶解度是60g;②冷却热饱和溶液;③B、C;(2)38.8g.
点评:本题是对溶液知识的考查,重点是抓住溶解度的实质,只要结合图表所提供的信息,分项探讨即可解决.

练习册系列答案
相关题目
 (2010?西宁)(1)如图是甲、乙两种固体物质的溶解度曲线.根据图示回答:
(2010?西宁)(1)如图是甲、乙两种固体物质的溶解度曲线.根据图示回答: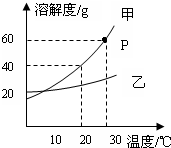 (2012?海珠区一模)(1)如图是甲、乙两种固体物质的溶解度曲线.
(2012?海珠区一模)(1)如图是甲、乙两种固体物质的溶解度曲线.

 (1)如图是甲、乙两种固体物质的溶解度曲线.根据图示回答:
(1)如图是甲、乙两种固体物质的溶解度曲线.根据图示回答: