题目内容
(2005?崇明县一模)(A组)在室温时,向饱和碳酸钠溶液中不断滴加盐酸,以下能正确表示溶液PH值与盐酸滴加量的关系的是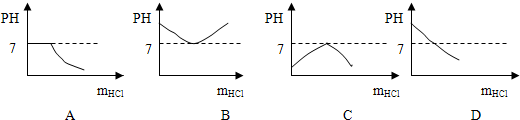
D
D
.
分析:主要从碳酸钠溶液呈碱性以及与盐酸反应是的溶液酸碱性的变化分析即可,主要利用了碱性溶液中性溶液及酸性溶液的pH分别是大于7、等于7、小于7.
解答:解:碳酸钠为碱性物质.溶液pH大于7,并能与盐酸反应生成氯化钠与二氧化碳和水,当滴入的盐酸量较少时,溶液中的碳酸钠有剩余,溶液成碱性;随着盐酸的滴加溶液碱性不断减弱,pH变小,当滴入的盐酸与碳酸钠恰好完全反应时,溶液呈中性;当滴入的盐酸过量时,盐酸有剩余,溶液呈酸性pH小于7.
答:D
答:D
点评:本题以图形的形式考查碳酸钠与盐酸的反应.即考查了该反应导致溶液酸碱性的变化,又训练了学生辨别识图的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
