题目内容
73g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,求反应后所得溶液中溶质的质量分数.
分析:反应后所得溶液是氯化钠溶液,根据化学方程式NaOH+HCl=NaCl+H2O和盐酸中溶质的质量可以计算出生成氯化钠的质量,最后用氯化钠的质量除以所得溶液的质量乘以百分之百便可得反应后所得溶液中溶质的质量分数.
解答:解:盐酸中HCl的质量为73g×20%=14.6g;设反应生成的NaCl的质量为x.
NaOH+HCl=NaCl+H2O
36.5 58.5
.14.6g x
=
解得x=23.4g
以反应后所得溶液中溶质的质量分数为
×100%=11.7%
答:反应后所得溶液中溶质的质量分数为11.7%.
NaOH+HCl=NaCl+H2O
36.5 58.5
.14.6g x
| 36.5 |
| 14.6g |
| 58.5 |
| x |
解得x=23.4g
以反应后所得溶液中溶质的质量分数为
| 23.4g |
| 73g+127g |
答:反应后所得溶液中溶质的质量分数为11.7%.
点评:本题主要考查根据化学方程式计算和溶质质量分数的计算,难度不大.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
氯化钠是调味用的食盐的主要成分,也是重要的化工原料.电解食盐水可得氢氧化钠、氢气和氯气,写出电解食盐水的化学方程式 .
(1)海水中含有丰富的氯化钠,利用风吹日晒可以从海水中提取粗盐.风吹日晒的作用是 ;将含有较多杂质的粗盐溶解后,可通过 操作除去其中的泥沙等不溶性杂质.
(2)某化学兴趣小组的同学在实验室用氢氧化钠溶液与稀盐酸做探究实验.为探究反应后溶液中溶质的可能组成,同学们作出了如下猜想:
①你认为甲、乙同学的猜想都合理吗?如有不合理的请说明理由.
②请你提出一个与甲、乙同学不同的猜想.你的猜想是 .请设计简单的实验证明你的猜想成立.
(3)73g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数.
(1)海水中含有丰富的氯化钠,利用风吹日晒可以从海水中提取粗盐.风吹日晒的作用是
(2)某化学兴趣小组的同学在实验室用氢氧化钠溶液与稀盐酸做探究实验.为探究反应后溶液中溶质的可能组成,同学们作出了如下猜想:
| 甲同学的猜想 | 可能只有氯化钠 |
| 乙同学的猜想 | 可能含有氯化钠、氢氧化钠和稀盐酸 |
②请你提出一个与甲、乙同学不同的猜想.你的猜想是
(3)73g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数.
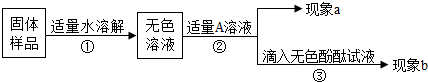
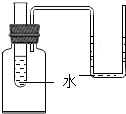 (2013?许昌一模)在学习酸和碱的知识时,王老师将几块氢氧化钠放在表面皿中,放置在教室的橱柜里,过了几天,表面皿中块状固体出现了许多白色粉末,同学们就此展开探究.
(2013?许昌一模)在学习酸和碱的知识时,王老师将几块氢氧化钠放在表面皿中,放置在教室的橱柜里,过了几天,表面皿中块状固体出现了许多白色粉末,同学们就此展开探究.